Wärmeentwicklung bei der Synthese von Hydrosilikaten im Porenbeton
SCHUHOV TECHNICAL STATEUNIVERSITY, BELGOROD, RUSSIAN FEDERATIONBei der Synthese von 11,3 Å-Tobermorit aus Kalk und Quarz beträgt die Wärmeentwicklung 125 kJ/kg und bei der Synthese von Xenolith 50 kJ/kg, wodurch Druck und Temperatur im Autoklaven ansteigen. Im Folgenden werden Empfehlungen für die Regelung der Hydratzusammensetzung bzw. zur Reduzierung des Dampfverbrauchs bei der Autoklavbehandlung gegeben.
1 Einleitung
1 Einleitung
Folgende Werte werden für die Reaktionsenthalpie und auch die Wärmekapazität von Tobermorit und dessen Zwischenphasen angenommen:
Angaben [1] in:
Die molare Standardentropie beträgt in
⇥kcal/Mol (bzw. kJ/Mol)
2 Berechnungen
Somit stimmt das theoretische Ergebnis zur Wärmeentwicklung beim Tobermorit mit den Werten von Babuschkin überein [1].
Nun wird die Temperaturerhöhung im Autoklav ermittelt: Dafür wird die spezifische Wärmekapazität von Tobermorit errechnet:
Hier ist m = 1 kg, woraus sich eine Temperaturerhöhung von ∆t 30,1 1,33 = 22,6° ergibt. Weil die Wärmekapazität von Tobermorit geringfügig höher ist als die Ausgangskomponenten, wird mit ∆t = 23 °C gerechnet.
Analog wird die Wärmeentwicklung bei der Synthese von Xenolith berechnet:
Rahimbaev [2] zeigt, dass die Änderung der Enthalpie unter isothermen Bedingungen mit einer geringen Änderung der Wärmeentwicklung im Bindungsystem einher geht. Daraus ergibt sich, dass die Wärmeentwicklung bei der Synthese von 11,3Å-Tobermorit, wie sie im Porenbeton bei der autoklavierten Härtung auftritt, viel mehr beiträgt als die des Xenoliths.
Die Wärmeentwicklung bei der Synthese von Tobermorit im Porenbeton, ruft eine lokale Temperaturerhöhung im Inneren des Materials auf 22-23 °C hervor.
3 Graphische Darstellung
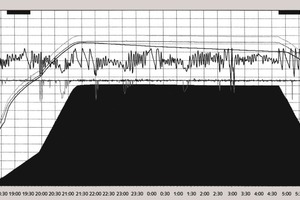
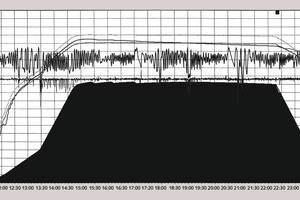
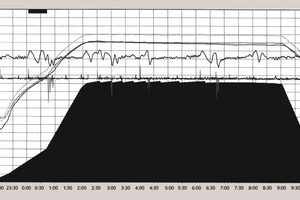
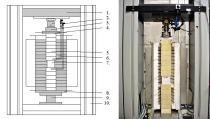
Die Analyse der Verläufe, die den Prozess im Autoklaven charakterisiert, zeigt Folgendes:
Bei der Autoklavbehandlung der Produkte mit der Dichte D 600 hält sich der Dampfdruck nach dem Erreichen des Arbeitspunktes stabil auf 1,1 MPa.
Bei der Autoklavbehandlung der Porenbetonprodukte mit einer Dichte von D 400 und 500, erhöht sich der Dampfdruck nach dem Erreichen des Arbeitspunktes auf 0,025-0,03 MPa. Dies schaltet nun die automatische Regulierung des Dampfdrucks im Autoklav ein, bzw. schaltet die Dampfversorgung aus, wodurch nach einigen Minuten der Druck bis zum eingegebenen Wert von 1,1 MPa absinkt. Danach steigt der Druck im Autoklaven wieder an, bis die automatische Regulierung sich erneut aufschaltet.
Die Anzahl der Ein-Ausschalt-Zyklen der automatischen Regulierung variiert zwischen 2 und 7, während die Intervalle zwischen den Zyklen zwischen 15 und 20, sogar bis 150 Minuten betragen. Ein gesamter Zyklus dauert zwischen 2 und 3,5 Stunden.
Im Laufe der Zeit sinkt die Anzahl der Ein-Ausschalt-Zyklen. Wenn die ersten beiden Abschaltungen nach 15-20 Minuten erfolgen, treten die letzten beiden 40-50 Minuten nach der letzten Abschaltung auf.
Die Frequenz und die Amplitude der Ein- und Ausschaltungen der Dampfversorgung sind abhängig von der Menge an Kalk und dem Aluminiumpulver bzw. von der Aluminiumpaste. Das zeigt indirekt, wie die Erhöhung des Dampfdrucks im Autoklaven nicht nur von der Synthese der Silikathydrate, sondern auch von Aluminathydratphasen bedingt wird. Jedoch ist der Beitrag der Aluminathydratphasen in der gesamten Wärmebilanz offensichtlich relativ klein.
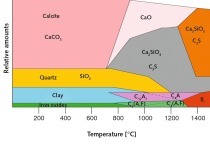
Eine steigende Enthalpie verschiebt die Reaktion in Richtung Xenolith und ein steigender Druck bzw. die Entropie in Richtung Tobermoritbildung. Offenbar übt der Faktor Energie einen vorherrschenden Einfluss aus, weshalb eine Verstärkung der Bedingungen im Autoklaven im System CaO-SiO2-H2O die Bildung von Xenolith begünstigt, aber beim Abkühlen der Betone bei hoher Feuchtigkeit sich wieder in Tobermorit zurück umwandelt [3].
4 Fazit
Daher wird für die Porenbetonherstellung empfohlen, die Produkte sofort nach der Entladung aus dem Autoklaven bis auf eine Restfeuchte nicht höher als 20 % zu trocknen, was auch zur Stabilisierung der nützlichen Phasenzusammensetzung beiträgt. Aufgrund der oben genannten Ergebnisse aus der Autoklavenbehandlung der Porenbetone mit der Dichte D 400 und D 500 ließe sich für die ersten 3–4 Stunden nach Erreichen des richtigen Arbeitspunktes der Dampfdruck bis auf 0,025-0,03 MPa reduzieren. Zusätzlich senkt die Wärmebildung bei der Synthese von Silizium- und Aluminathydraten Energiekosten um einige Prozente.

tab ZKG KOMBI Test
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.
tab ZKG KOMBI Study Test
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.