Hydrophobierung von Gips durch Silane (Teil 1)
TU BERGAKADEMIE FREIBERG // AKZO NOBEL CHEMICALS AGDer wesentliche Nachteil beim Einsatz von Gipsprodukten im Baubereich besteht in ihrer schlechten Wasserbeständigkeit. Diese lässt sich zwar durch die Zugabe von Spezial-Silanen verbessern, allerdings ist nur sehr wenig über die Wirkungsweise solcher Verbindungen bekannt. In diesem Bericht wird die hydrophobierende Wirkung von Propyltriethoxysilan als Beispiel eines kurzkettigen Alkylalkoxysilans in einer alkalischen Gipsmatrix ausführlich untersucht.
1 Einführung
1 Einführung
Mit den Untersuchungen, welche im Folgenden beschrieben sind, wird am Beispiel von Propyltriethoxysilan (PTES, n = 3) die Wirkung der Alkyltriethoxysilane [Si(OCH2CH3)3CnH2n+1], einer Gruppe der Silane näher aufgezeigt. PTES wurde ausgewählt, da erste Hinweise auf die hydrophobierende Wirkung in Abhängigkeit von der Alkylkettenlänge (n < 5) bereits vorlagen [9]. Alkylalkoxysilane mit einer kurzen Alkylkette sind demnach gut geeignet, um die Wasserbeständigkeit von alkalischen Gipsrezepturen zu erhöhen. Je kürzer die Alkylkette des Alkyltriethoxysilans, desto geringer ist die Wasseraufnahme des Gipsproduktes. Mit Methyltriethoxysilan wurde die geringste Wasseraufnahme bestimmt. Die Wasseraufnahme bei Verwendung von Octyltriethoxysilan ist von gleicher Größenordnung wie die Wasseraufnahme unbehandelter Gipserzeugnisse [9].
Wie allgemein bekannt, reagieren Alkyltriethoxysilane in Anwesenheit von Wasser zu Silanolen und anschließend zu Siloxanen. Beide Reaktionen werden durch Säuren sowie Basen katalysiert. Im Fall der Gipsbaustoffe ist die basisch katalysierte Reaktion eher von Bedeutung, da einige Produkte, wie z.B. Gipskalkputze, bereits alkalisch sind. Die Hydrolysereaktion von Propyltriethoxysilan (n = 3) beginnt gemäß Reaktion 1 mit dem Austausch einer Ethoxy-Gruppe gegen eine Hydroxy-Gruppe. Dieser Schritt stellt eine nukleophile Substitutionsreaktion nach SN2 [10] (R = Propyl) dar:
Auf Basis dieser Kenntnisse wurden detaillierte Untersuchungen anhand von Hydrophobierungstests an Gipsoberflächen, NMR-Messungen (Teil 1) und Adsorptionssimulationen (Moleküldynamik, Teil 2) durchgeführt, um ein besseres Verständnis zum Mechanismus der hydrophobierenden Wirkung von Propyltriethoxysilan (PTES), als ein Vertreter der kurzkettigen Alkyltriethoxysilane, zu erhalten.
2 Substanzen und Methoden
Für den Nachweis der Silanspezies mittels 29Si-NMR-Spektroskopie waren höhere Konzentrationen als 0,5 %-Gew. in einer wässrigen Lösung nötig. Da sich Propyltriethoxysilan mit Wasser nicht mischen lässt, wurde es im Verhältnis 1:1 mit Ethanol vermengt. Einige Tropfen Salzsäure (pH-Wert: 1) bzw. Natriumhydroxidlösung (pH-Wert: 14) wurden zur Katalyse sowohl bei niedrigem als auch bei hohem pH-Wert zu 3 mL der Silan-Ethanol-Mischung beigemengt. Es resultierten die pH-Werte 3 und 12,5 (pH-Elektrode, Typ: ROSS, Orion).
Sämtliche NMR-Spektren wurden mit einem DPX-400 (Bruker) aufgenommen. Die Kernresonanzfrequenzen liegen bei 100,6 MHz für 13C bzw. 79,49 MHz für 29Si. Als Insert wurde deuteriertes Benzol zusammen mit dem Standard Tetramethylsilan (TMS) zugegeben. Die Spektren wurden mit dem Softwarepaket Topspin 2.1 (Bruker) ausgewertet.
3 Ergebnisse und Diskussion
Mit zunehmendem Propyltriethoxysilan-Gehalt sinkt demnach die Wasseraufnahme deutlich, wobei die Versuche nur einen geringen Prozentbereich an Silangehalten abdecken. Höhere Gehalte an PTES als 1,33 Gew.-% wurden nicht untersucht, da diese für industrielle Anwendungen nicht mehr wirtschaftlich relevant sind.
Bei Verwendung des Alkyltriethoxysilans OTES wurde keine Reduzierung der Wasseraufnahme beobachtet. Die zur Absorption des Wassertropfens benötigte Zeit war identisch mit der einer ausgehärteten Gipsoberfläche ohne OTES nach Aberle u.a. [9]. OTES wurde daher in nachfolgenden Versuchen nicht mehr berücksichtigt.
Die hydrophobierende Wirkung des PTES wurde weiterhin mit einem konstanten Gehalt von 0,165 Gew.-% in Abhängigkeit von der Verarbeitungszeit des Gips-Frischmörtels untersucht. Unterschiedliche Verarbeitungszeiten wurden durch den Einsatz von variierenden Mischungen aus a-Halbhydrat und b-Halbhydrat realisiert, da die Verarbeitungszeit eines Frischmörtels aus a-Halbhydrat länger ist im Vergleich zu der eines b-Halbhydrats. Auf den Einsatz von Verzögerungs- bzw. Beschleunigungsmitteln wurde bewusst verzichtet, um den möglichen Einfluss dieser Stoffe auf die Wirkung des Silans auszuschließen. Die Verarbeitungszeit von reinem a-Halbhydrat (mit 0,5 Gew.-% Ca(OH)2) wurde durch die sukzessive Zugabe von b-Halbhydrat von 15 Minuten auf wenige Sekunden verkürzt. Über den anschließenden Wassertropfentest wurde eine zunehmende Hydrophobierung mit Verlängerung der Verarbeitungszeit beobachtet (Bild 3).
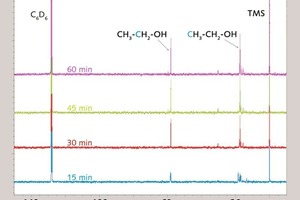
Dieses Ergebnis führte zu der Annahme, dass es zwischen der Hydrolysezeit von PTES und der maximalen Hydrophobizität des verarbeiteten Gipses einen Zusammenhang gibt. Um diese Annahme zu bestätigen, wurde die Hydrolysezeit durch eine Vorhydrolysereaktion von PTES, von zwischen 5 und 60 Minuten in einer Ca(OH)2-Suspension (mit 0,5 Gew.-% Ca(OH)2 bezogen auf das Halbhydratpulver) verlängert. Diese Suspension wurde im Anschluss an die unterschiedlichen Vorhydrolysezeiten als Anmachwasser (Anmachsuspension) benutzt. Auf diese Weise konnte ein „Zeitfenster“ für die Hydrolyse von bis zu 75 min (60 Min. Vorhydrolyse + 15 min Verarbeitungszeit des Frischmörtels, aus reinem a-Halbhydrat) erreicht werden. Wie aus Bild 4 ersichtlich, tritt eine maximale hydrophobierende Wirkung bei einer Hydrolysezeit von 35 min auf (PTES-Gehalt stets 0,165 Gew.-%). Anschließend fällt die hydrophobierende Wirkung wieder ab. Entsprechend der 29Si-NMR-Spektren treten im Zeitfenster zwischen 30 und 45 Minuten Kondensationsprodukte auf, was vermutlich zur Reduzierung der hydrophobierenden Wirkung führt.
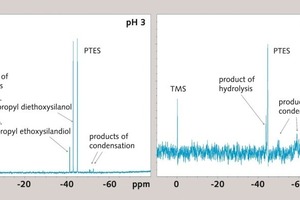
Bild 6 zeigt die 29Si-NMR-Spektren für PTES bei pH-Wert = 12,5 nach 35 Minuten Hydrolysezeit. Von den drei möglichen Hydrolyseprodukten (-ol, -diol, ‑triol) wurde nur eines nachgewiesen, bei welchem es sich in Anlehnung an die 29Si-NMR-Spektren von Tetraethoxysilan (TEOS [20]) um Propyldiethoxysilanol handeln sollte (das Hydrolyseprodukt aus Reaktion 1). Die Signale weiterer Hydrolyseprodukte weisen im Vergleich zum eingesetzten Silan einen größeren Unterschied in der chemischen Verschiebung auf. Im PTES-Spektrum (Bild 6, rechts) erscheinen nach 35 Minuten rechts vom ursprünglichen PTES-Signal die Signale von Kondensationsprodukten.
Die Messung wurde bei pH 3 wiederholt, um die PTES-Hydrolyse auch bei diesem pH-Wert näher zu betrachten. Nach Bild 1 [14, 19] sollte bei einem sauren pH-Wert die Hydrolysereaktion schneller als die Kondensationsreaktion ablaufen. Wie aus dem Spektrum ersichtlich (Bild 6, links), treten bei pH 3 zwei der drei möglichen Hydrolyseproduktsignale nach 35 min auf. Diese sind die Signale von Propyldiethoxysilanol und Propylethoxysilandiol. Somit bestätigt sich das bei pH = 12,5 auftretende Signal als das von Propyldiethoxysilanol (kleinste Verschiebung gegenüber PTES; das –diol und das –triol erscheinen bei einer größeren Verschiebung Richtung PTES). Der Unterschied der chemischen Verschiebung in den Spektren bei saurem bzw. basischem pH-Wert lässt sich durch die Deprotonierung des Silanolmoleküls bei pH 12,5 [21] erklären.
In Zusammenfassung aller bisher vorliegenden Ergebnisse scheinen Hydrolysespezies wie Propyldiethoxysilanol die hydrophobierende Wirkung von alkalischem Gips zu bewirken, insbesondere wenn die Verarbeitungszeit im Bereich von ca. 35 min liegt. Wird dieses Zeitfenster und damit die Hydrolysezeit überschritten, bilden sich Siloxan-Kondensationsprodukte in der wässrigen Lösung in einem solchen Maß aus, dass der verarbeitete Gips nur noch unwesentlich hydrophobiert wird.
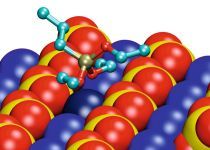
Im Teil 2 (ZKG 9/2013) schließt sich die molekulare Simulation (Moleküldynamik) an, mit deren Hilfe Wechselwirkungen der Silane mit kristallinen Gipsoberflächen auf molekularer Ebene beschrieben und analysiert werden. Die Ergebnisse werden zusammen mit den bisher erhaltenen experimentellen Ergebnissen bewertet und zusammengefasst.

tab ZKG KOMBI Test
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.
tab ZKG KOMBI Study Test
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.
Es handelt sich hierbei um ein Testangebot. Es berechtigt zu keinem gültigen Abonnement und steht hier rein für Testläufe. Bitte diesem Prozess nicht folgen.

![Relative Reaktionsgeschwindigkeit vrel der Hydrolyse- und Kondensationsreaktionen von Silanen in Abhängigkeit vom pH-Wert [15, 20]](https://www.zkg-online.info/imgs/tok_c87ce0002aa8d6b55597e6ef584b661b/w300_h200_x400_y306_101535921_9c0bda7409.jpg)